這邊分享我自己筆記的小部落格,走到今天也收到不少人的回饋。很感謝大家指出我誤植的部分,甚至是一堆錯字。在這裡除了感謝還是感謝,就算只是單純告訴我需要勘誤的地方,也讓我知道還是有人一個字一個字讀這些得來不易的整理,也成就我努力的動力!也希望大家日後如果有發現任何寫不對或者有疑問的點,都可以繼續利用粉絲團提出來唷!
以往接觸到AF的病人,往往在想原因的時候大家都不會漏掉甲狀腺,但這樣一個在全身都可以作用的賀爾蒙到底又是怎麼影響心臟呢?心衰竭和心肌梗塞跟甲狀腺其實也是有關係的!這兩篇review提供了其背後一個基本的認識,甚至未來有可能用在心肌梗塞後的心臟保護治療。
甲狀腺的轉換酵素
Deiodinase 在身體中共有三型,後面文章就直接縮寫為D1,D2,D3
D1 在周邊組織含量豐富,負責血液循環中的T4轉換成T3
D2 在下視丘,腦部和腦下垂體以及Brown fat含量多,對T4親和性特高,在周邊循環以及細胞內將T4轉為T3
D3 主要存在於胎盤,腦部,皮膚,主要代謝並終止T3,T4的活性
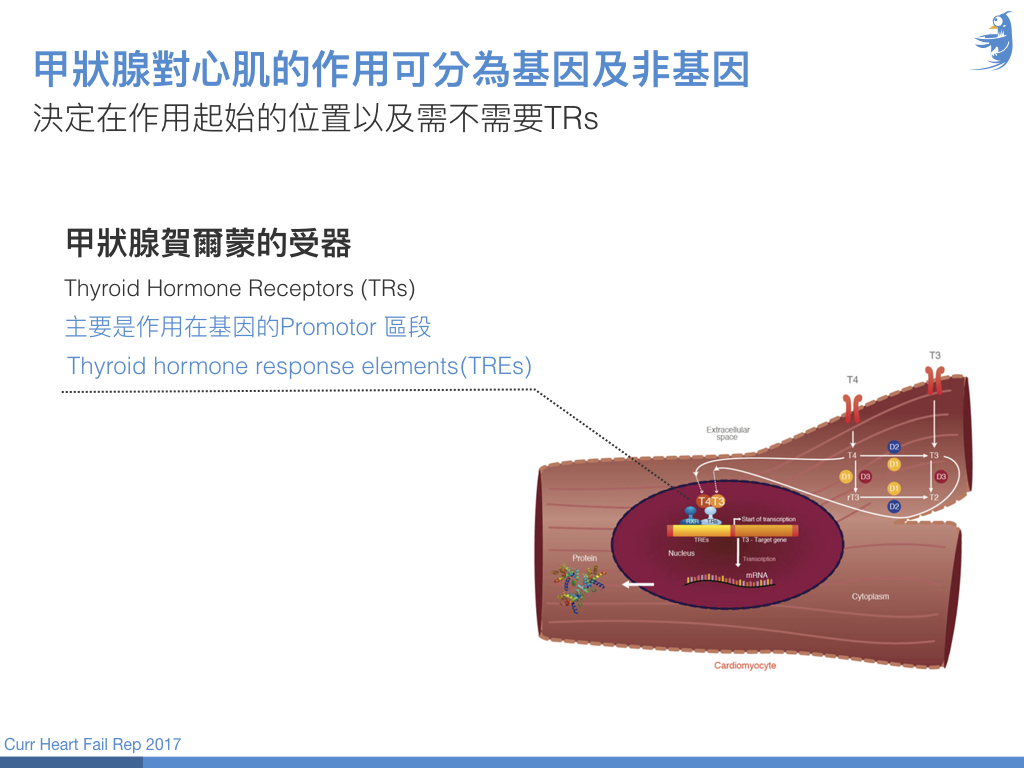
甲狀腺在心肌細胞的影響
甲狀腺可以透過基因調節,控制SERCA2 和 PLN的表現,影響鈣離子的再吸收與釋放,正向影響新機舒張,調整Myocin heavy chain的製造增加收縮,正向調控Beta-1 接受器達到 inotropic的強心效果。透過基因及非基因的路徑,影響細胞膜上面的鈉,鉀,鈣離子通道,達到chronotropy的心跳加速效果。而基因及非基因的路徑,其實在後端走的路徑有時候是重複的。
甲狀腺的接受器主要有幾個分型,重要的兩種就如下圖所示,文中直接簡寫為THR或TR
透過增加NO的製造,以及改善小動脈的鈣離子再吸收功能,甲狀腺也能讓平滑肌舒張,進而降低系統血管阻力(systemic vascular resistence)。
由於系統血管阻力的降低,加上直接的強心(Inotropic)效果,心輸出量上升。而在血管阻力降低的同時,腎臟的灌流也暫時下降,於是這樣一來RAAS系統也接著啟動,造成Volume(Preload)增加,也貢獻了心輸出量。
心血管疾病的風險
首先來定義一下甲狀腺的亢進跟低下
甲狀腺機能低下
對於血脂代謝的影響,Overt Hypothyrodism是相當明顯的,但subclinical在研究中的結果卻不是很一致。主要還是影響肝臟減少LDL接受器的表現。不過RCTs到Meta-analysis到考科藍的系統分析並沒有很強力的支持治療Subclinical Hypothyrodism來達到降血脂的效果。
甲狀腺機能亢進
對於血壓和血管功能的影響,同樣的,相較Overt Hyperthyroidism明顯的高血壓,subclinical hyperthyroidism 對血壓的影響就不是那麼明確。
在血管內皮的影響方面,值得注意的是,在甲狀腺自體免疫造成的甲狀腺功能低下病人身上,給予甲狀腺補充並沒有辦法完全改善內皮細胞的功能異常。這暗示著抗甲狀腺的自體抗體也可能是造成內皮細胞受影響的原因(另外就是同時慢性的低度發炎)。
自體抗體以及失調的血脂也都被認為可能降低血管內皮endothelial nitric oxide synthase的表現,進而造成動脈無法舒張。
甚至連MI的比率和主動脈鈣化率,也都和自體抗體有關聯。
在血栓的形成方面,甲亢在臨床上造成的實際影響仍不確定。但Subclinical Hypothyrodism可能是thrombogenic,實驗有發現這一群病人antithrombin III較低的活性,以及較高的Fibrinogen,Factor VII,plasminogen activator inhibitor antigen。但目前這仍然是探索中的問題,所以表格裡面還是寫了一個Uncertain。
心衰竭
心肌細胞對循環中的甲狀腺賀爾蒙相當敏感。賀爾蒙改變可以引發心衰竭,而心衰竭本身也可以改變賀爾蒙的平衡。即使是輕度甲狀腺不足的人,心衰竭的機會也會增加。
Low T3 syndrome (euthyroid syndrome)
周邊血液T4到T3的轉換失調,造成低T3,高rT3,正常的T4以及TSH。這症候群在住院病人,Critical的病人裡常見,在心衰竭的病人裡面有20-30%的病人會出現。
出現了Low T3 syndrome以及subclinical hypothyrodism在心衰竭的預後是最差的。
目前出現這症候群的解釋假說包括:
#Deiodinases酵素的活性改變:T3濃度變低,沒或性的rT3反而開始累積
#THS分泌下降:superior cortical centers 的抑制訊號使TRH的分泌量下降
心衰竭甲狀腺素的補充:只在出現Low T3或者subclinical hypothyrodism的時候考慮。
目標是維持臨床和生化上面的euthyroid states。要避免比生理劑量更大的甲狀腺素給予,也就是每天不要超過0.2–0.4 μg/kg (15–30 μg 每天,一天兩到三次) 和大約 1 μg/kg 每天的 levothyroxine (50–100 μg 每天一次)。
心肌梗塞
甲狀腺賀爾蒙的改變會在心絞痛發生的三天內開始發生,最大的改變會在第24-36小時。
15-20%表現low T3 syndrome,10%的人表現出subclinical hypothyroidism。但目前這樣的改變究竟是位於心肌梗塞前,還是心肌梗塞造成的結果尚不知道。
如同在心衰竭的族群中觀察到的,D3的活性增加,D1D2的活性下降,可能是甲狀腺濃度改變的原因。理論上這樣子降低細胞的代謝率在MI的狀況下應該是有好處的,但實際上卻發現MI的病人如果出現甲狀腺賀爾蒙的變化,其癒後會更差。甚至心肌梗塞後的T3濃度,和心室的功能恢復在兩天和六個月的時間點都有強烈關聯(一個晚期恢復的指標)。
心臟的保護效果
下面的內容來自觀察研究以及動物實驗,尚未推及臨床使用。但考慮到甲狀腺失調對心臟造成的不良影響,未來或許可以就這些發現的內容,發展出心臟保護的療法(Cardiopertection)。
發展心臟保護療法的目的在於降低或限制心臟在心肌梗塞時受到的傷害,也避免進一步影響LV供能,更防止再進展到不可逆的心衰竭。
心臟在心肌梗塞時受到的傷害主要來自:梗塞時的缺氧傷害和梗塞後的再灌流傷害。
保護的效果則需要多種機轉的同時幫忙,包括
#刺激細胞生長(stimulation of cell growth)
#血管增生(neoangiogenesis)
#代謝的適應與調適(metabolic adaptation),維持粒線體的完整性(mitochondrial integrity)
而近來的研究顯示,甲狀腺可能可以扮演這樣的角色,包括限制梗塞近端區域的壞死,還有其抗纖維化以及促進血管增生的特性可以對抗梗塞近端以及遠端區域的Remodelling。
動物實驗就發現,缺少卡路里能量的心肌細胞,出現有點類似低甲狀腺時會發現的情況,SERCA2 跟 Myocin heavy chain alfa 都會被影響。而給予T3補充之後心功能則會改善。這可以說明甲狀腺素在慢性疾病時的角色。然而在急性期的時候,迅速恢復SERCA2的功能也可能有其風險,他對ATP缺乏相當敏感,特別是在缺氧-再灌流,粒線體功能異常,這時使用T3去恢復SERCA2是不是好事就得打個問號了。
另外甲狀腺可以限制梗塞的範圍擴張,透過活化細胞存活路徑 PI3K/AKTt, protein kinase C 同時抑制 p38 MAPK 。但超過生理的過高劑量也是會增加死亡率。
心肌梗塞早期的T3也可以減緩p53在border zone上升濃度,如此一來可以減少缺氧-再灌流造成的粒線體功能異常,細胞凋亡(apoptosis),細胞壞死(necrosis)的程度。另外T3的治療可以誘發hypoxia inducible factor 1α (HIF1A)的表現,並減少再灌流的傷害。
在MI的遠端的非壞死區域,長時間的T4治療可能對於心肌細胞以及血管的collagen matrix remodelling有好處。
甚至,甲狀腺賀爾蒙也透過基因以及非基因的方式,有免疫調節的效果。體外實驗的T3就可以在人類osteoblastic-like cells以及bone marrow stroma cell 增加IL-6,IL-8的濃度(但使用超過生理劑量),在老鼠細胞則會增加IL-12。而在心肌梗塞發生後的發炎過程,可能就有甲狀腺介入的角色。
Reference
Nature Review Cardiology, Volume 14 January, 2017
Thyroid hormones and cardiovascular
disease Avais Jabbar
doi:10.1038/nrcardio.2016.174
Curr Heart Fail Rep 2017
Thyroid Dysfunction and Heart Failure: Mechanisms
and Associations
Hernando Vargas-Uricoechea
Hernando Vargas-Uricoechea
DOI 10.1007/s11897-017-0312-5

















沒有留言:
張貼留言